2024年3月15日
2024年3月15日
黄烷-3-醇是茶树幼叶主要多酚类化合物,在茶树中参与其生物合成的酶已得到了广泛的研究,然而这些功能酶在细胞中的定位被忽视。
3月10日,The Plant Journal在线发表了安徽农业大学王云生团队题为“A flavonoid metaBolon: cytochrome B5 enhances B-ring trihydroxylated flavan-3-ols synthesis in tea plants”的研究成果。文章中利用空间代谢组揭示了B环三羟 基黄酮类化合物分布模式,通过亚细胞定位和蛋白互作分析确定了其生物合成途径中关键酶,本研究为了解茶树类黄酮多样性和高效合成机制提供了有价值的见解。迈维代谢为其提供空间代谢组检测与分析服务。

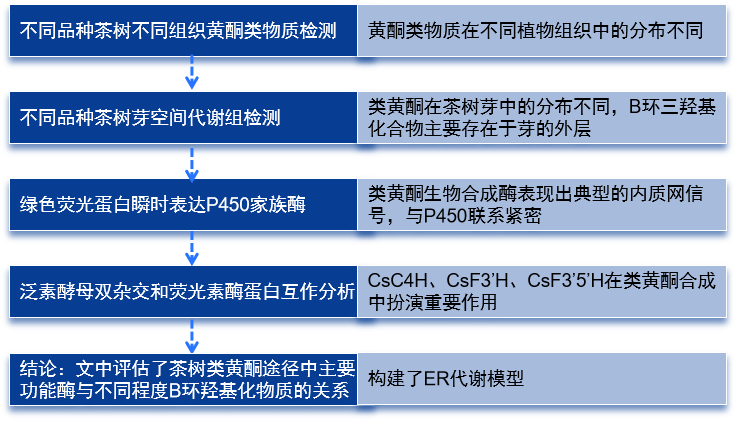
研究思路:
研究结果:
1.类黄酮在茶树中的积累规律
为研究黄酮类化合物分布规律测定了不同品种(舒茶早、黄金芽、紫鹃茶)不同组织(芽、幼叶、成熟叶、老叶、幼根、幼茎)中黄烷-3-醇、黄酮醇、花青素和原花青素(PAs)含量。老叶中黄烷-3-醇的含量明显低于幼叶。此外,SCZ幼叶中黄烷-3-醇含量显著高于HJY和ZJ。黄酮醇及其衍生物主要在老叶中积累,花青素主要在ZJ叶中积累。可溶性PAs在叶片中的积累浓度为不溶性PAs 10倍,可溶性PAs主要积累在茎中,不溶性PAs主要积累在幼根中。综上所述,茶树在不同组织中积累多种黄酮,以黄烷-3-醇为主要成分。
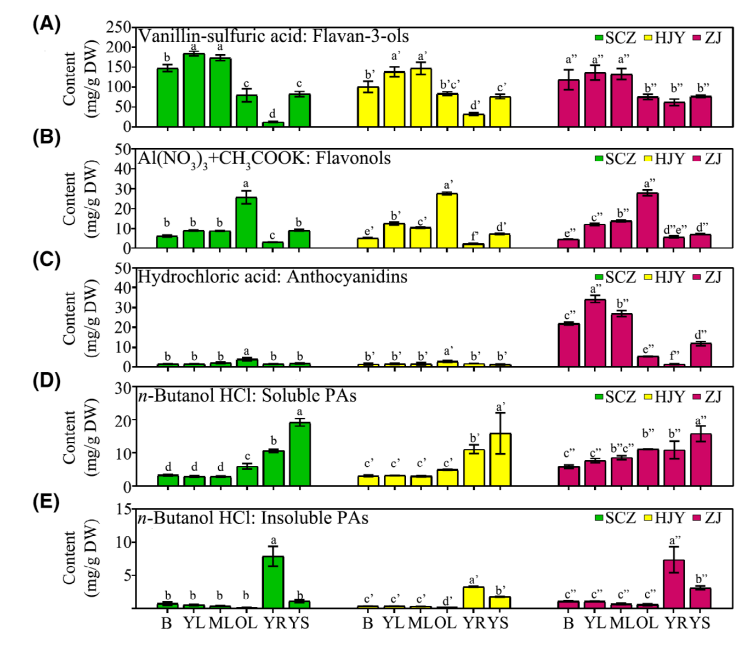
茶树中类黄酮积累概况
2.不同B环羟 基黄烷-3-醇含量和空间分布变化
对不同叶片颜色茶树芽进行黄烷-3-醇分析,SCZ、HJY和ZJ普遍存在B环三羟 基黄烷-3-醇,且为最丰富的黄酮。随后,检测了各种羟 基黄酮类化合物在茶树芽切片中的空间分布。类黄酮在茶树芽中的分布不同,原花青素B2/B3(PAs B2/B3,m/z = 577.1313)在芽内层表现出更强的信号,B环三羟 基化合物主要存在于芽的外层。
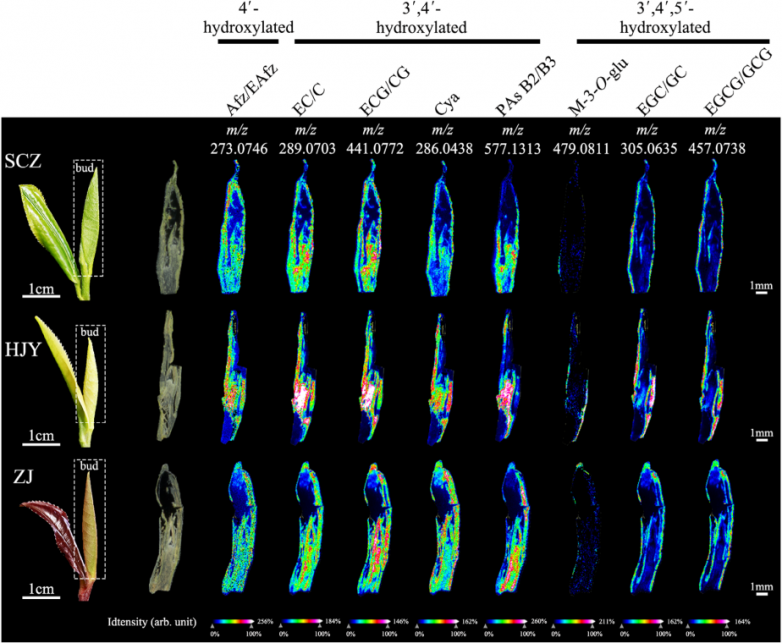
不同B环羟 基化合物在芽中的空间分布
3.与类黄酮途径相关的基因表达
文中检测了芽、幼叶、成熟叶、老叶、幼茎和幼根中11个类黄酮生物合成酶基因。CsC4H在幼叶和根中表达水平相对较高。芽和幼叶转录水平最高,并随着叶片成熟逐渐降低,幼根和老叶的转录水平最低。CsF3’5’H在芽中的表达量最高,在老叶中很低。
4.类黄酮途径酶的亚细胞定位
本研究探讨了与类黄酮代谢途径相关酶的定位。CsC4H、CsF3’H和CsF3’5’H被归入细胞色素P450家族,这些酶可能存在跨膜结构域。为验证这些类黄酮P450酶的胞内定位,文章利用绿色荧光蛋白(GFP)在本氏烟草叶表皮细胞中瞬时表达以确定这些酶定位结果。结果显示参与类黄酮生物合成的酶(CsCHS、CsCHI、CsF3H和CsDFR)表现出典型的内质网信号,表明它们可能与细胞色素P450的联系更为密切。
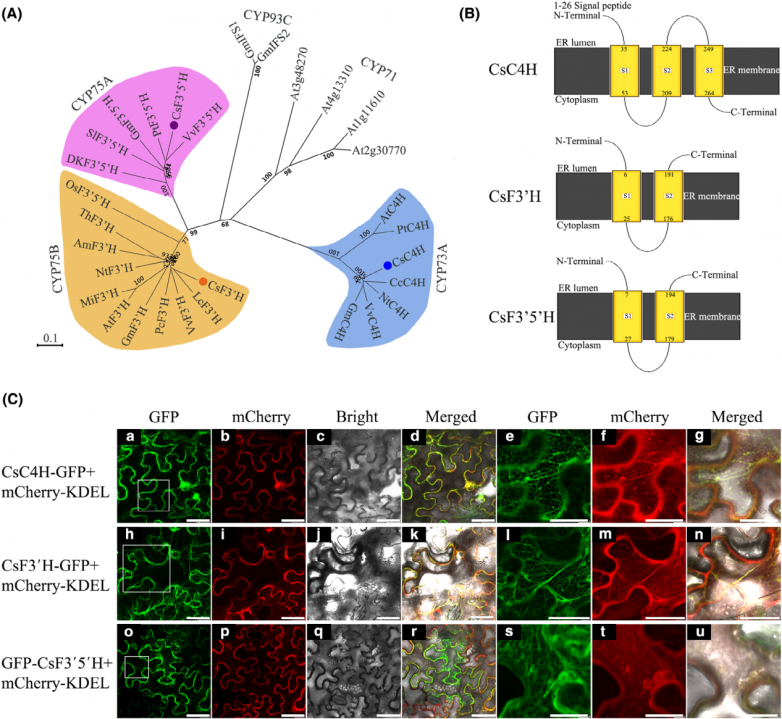
类黄酮途径酶亚细胞定位结果
5.类黄酮途径P450酶互作关系
通过泛素酵母双杂交(SU-Y2H)和荧光素酶蛋白互作分析(Split-LUC) 研究了CsC4H、CsF3’H和CsF3’5’H的潜在相互作用,结果显示CsC4H、CsF3’H和CsF3’5’H之间没有直接的相互作用,CsF3’5’H蛋白C端参与了黄烷-3-醇代谢物的形成。结合SU-Y2H和split-LUC结果证实这三种P450酶在体内相互关联,但似乎在物理上没有相互作用。
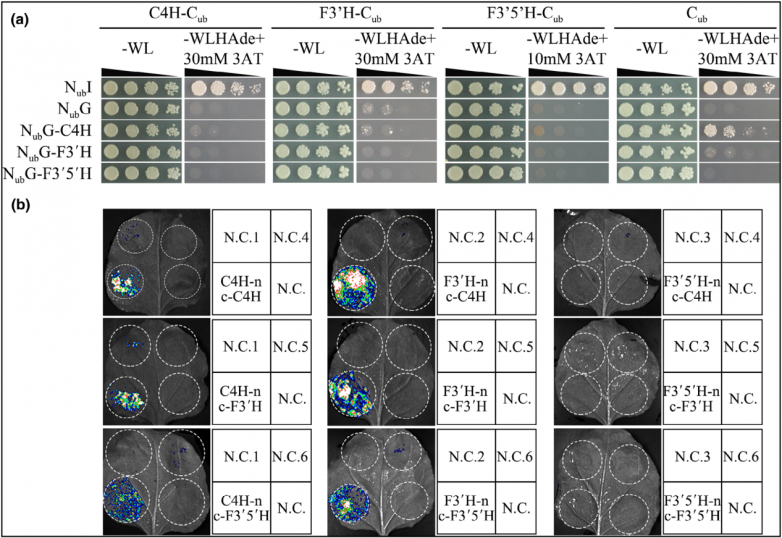
类黄酮途径蛋白空间邻近性及相关性
6.与类黄酮可溶性酶相互作用的P450酶
文中进一步研究了三种P450酶与代谢物形成相关可溶性蛋白的互作关系。类黄酮生物合成P450(CsC4H和CsF3’H)可以与除CsLAR外的大多数可溶性酶发生物理相互作用。然而,合成B环三羟 基黄烷-3-醇的P450酶CsF3’5’H仅与上游酶(CsCHS、CsCHI和CsF3H)存在空间关联,没有直接相互作用。
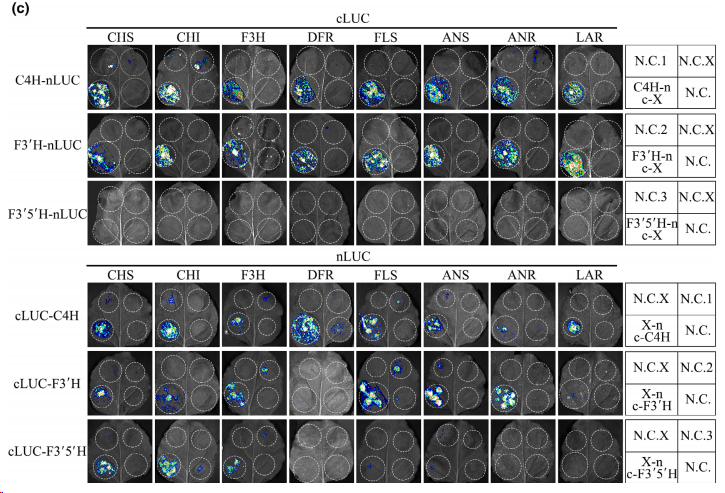
烟草叶片中P450酶与类黄酮途径可溶性酶空间位置关系
7.细胞色素B5与P450物理相互作用并支持CsF3’5’H催化能力
接下来,文中通过SU-Y2H和split-LUC方法评估了P450和三种CsCB5之间的相互作用。结果显示,CsCB5A、CsCB5B和CsCB5C直接与CsC4H、CsF3’H和CsF3’5’H相互作用,CsCB5C和CsF3’5’H的ß-半乳糖苷酶活性明显强于其他2种CsCB5s。在WAT11酵母菌株中进行了CsCB5s和P450s异源共表达,结果表明CsC4H和CsF3’H催化活性并不依赖于CsCB5蛋白。另外研究表明CsCB5C是CsF3’H催化反应不可或缺的合作伙伴,提高了CsF3’H在合成相应产物中的催化活性。
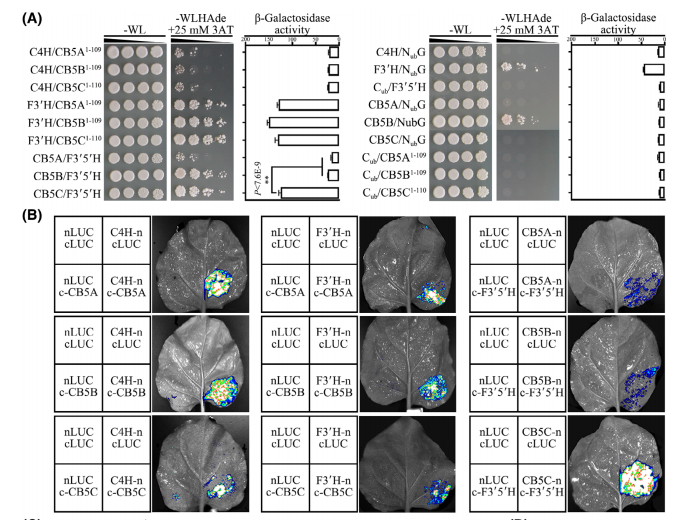
CsCB5蛋白与类黄酮生物合成途径P450酶的关系
8.CsCB5C是类黄酮合成的电子穿梭蛋白
文中用丙氨酸(Ala)取代一个或两个保守的组氨酸残基(His-39和His-73),生成位点突变的CB5C(CsCB5C-CΔ1、CsCB5C-Δ2和CsCB5C-Δ1Δ2)。SU-Y2H结果显示,组氨酸残基突变不会降低CsF3’5’H物理结合能力。在酵母菌株WAT11中共表达CsCB5C-CΔ1、CsCB5C-Δ2或CsCB5C-Δ1Δ2,结果表明,CsCB5C中两个组氨酸残基作为电子载体的性质非常重要,影响了CsF3’5’H催化活性。
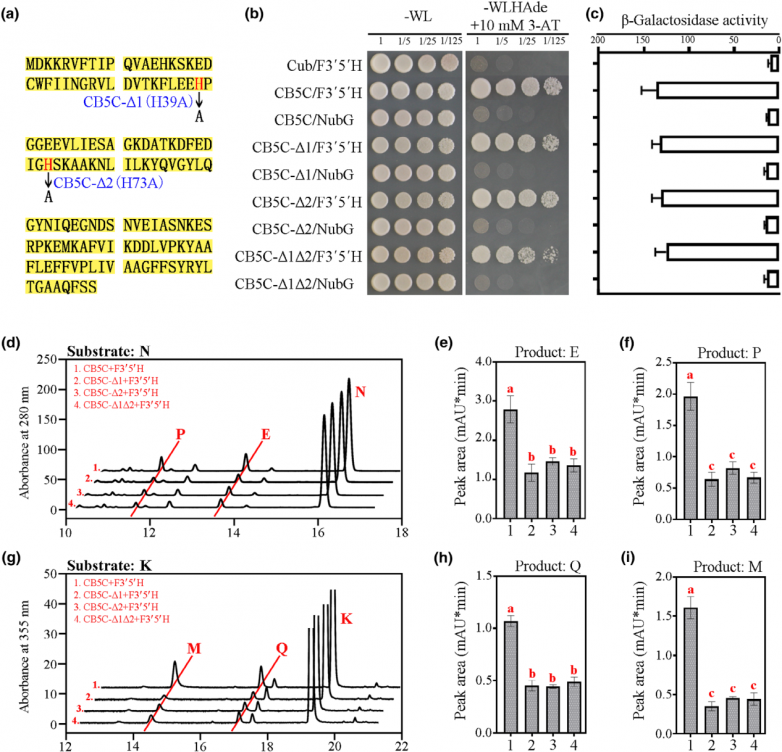
CsCB5C蛋白影响CsF3’5’H催化活性的关键位点
研究结论:
文中评估了茶树类黄酮途径中主要功能酶与不同程度B环羟 基化物质的关系。此外,构建了一个ER代谢模型,该模型由CsC4H和CsF3’H串联组成,CsCPR作为电子供体蛋白以产生B环二羟 基黄酮类化合物。几种可溶性酶通过弱力附着在P450酶的细胞质表面。这些可溶性酶之间的相互作用可以调节不同代谢途径的代谢产物。在CsF3’5’H的参与下,上游产物被催化为B环三羟 基中间产物,然后通过可溶性酶产生各种下游类黄酮化合物。
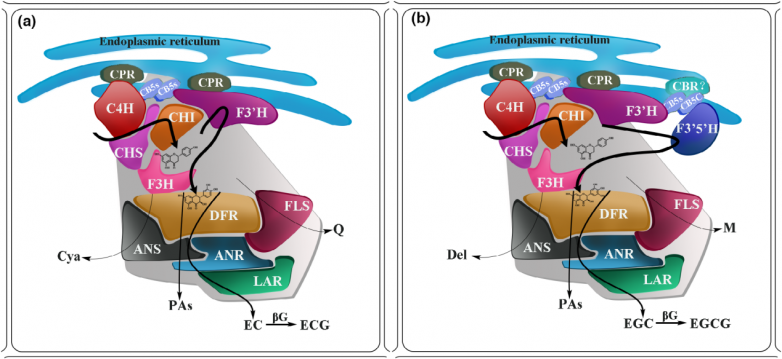
山茶中类黄酮生物合成模型。
迈维代谢现推出植物激素空间质谱成像技术,助力您的文章发表,欢迎垂询!